|
FDA在2022年10月21日发布了外用制剂仿制药IVPT技术指南草案《In Vitro Permeation Test Studies for Topical Drug Products Submitted in ANDAs》

该技术指南草案将外用制剂仿制药IVPT研究过程中的方法开发、方法验证和数据统计方法等方面做了较为详尽的阐述。该指南草案与我司在2019年基于ICH各国指南及学术文献所制定的内部研究方案和标准差异不大,且已通过CDE技术审评,在此不再赘述。
本文想重点聊聊FDA该指南草案之外的一些延伸思考。
1.IVPT中的皮肤表面温度只需要控制在32±1°C范围吗?
FDA指南上给出了在IVPT研究中,皮肤表面温度建议控制在32±1°C范围内,以模拟皮肤正常生理温度。这是常规要求,我们也要基于科学的态度来考虑一些特殊情况:
(1)创新药
对于一些治疗和缓解疼痛的外用制剂,部分患者喜欢用加热垫、电热毯、桑拿或热水浴等来缓解疼痛。但这无意中有可能导致外用药物中活性成分递送量意外增加,从而可能潜在的影响药物对于人体的全身暴露量,进而影响到药物安全性。身体加热已被证明会导致芬太尼、尼古丁、硝酸甘油和三硝酸甘油酯的血浆水平升高。因此不仅要考虑皮肤表面在32°C条件下,药物释放和吸收的速率和程度,同样也要考虑在更高皮肤表面温度条件下(例如37°C等)药物释放和吸收,来确保药物对于人体的应用安全性。对于窄治疗窗的药物或者对药物全身暴露量增加敏感的易感患者群体尤其更要引起重视,避免构成潜在的安全问题。对此应关注药物释放设计或说明书中予以重点说明。
(2)仿制药
例如Voltaren® 凝胶已在说明书描述了对人体进行了热应用研究。这项研究报道,使用前将药物前适度加热15分钟,全身吸收没有临床相关差异。那么对于仿制药的开发,应当保证使用前将药物适当加热的操作,对于受试制剂和参比制剂的药物释放应保持一致性(也应包括制剂稳定性一致),因此建议在IVPT研究中将皮肤表面温度适当升高后,再次将受试制剂和参比制剂进行对比研究。
2.对于半固体制剂,IVPT中上药后供体池顶部不封口会怎样?
与贴膏剂具有背衬膜保护所形成的封闭环境不同,半固体制剂在IVPT供体池在上药后,顶部是暴露在空气中的。制剂中挥发性成分(特别是挥发性溶剂)的蒸发会改变这些半固体制剂的组成和性能。
溶剂的蒸发会加快药物的饱和状态进程,然后导致药物沉淀。这里面主要涉及两个过程,初始阶段由于接受池供热,供体池药物温度升高,导致半固体药物粘度降低、药物溶解度增加和挥发性溶剂快速蒸发。所有这些因素都会导致药物的热力学活性增加,进而驱动局部药物渗透的动力学,导致药物渗透增加。但后期由于药物的过饱和或溶剂耗尽所导致的药物沉淀或结晶,这种优势就会消失,药物递送和渗透率将会减慢。在通量分布曲线上的表现就是开始时半固体制剂的通量迅速上升,比相应的基线通量分布更早达到 Jmax,通量的这种快速上升之后是稳步下降,直到达到一个平台,导致圆顶形的通量分布曲线。
因此建议在IVPT研究中,在供体池上药后,顶部盖上配套的塞子或用高分子薄膜进行覆盖(但要与外界保持适当的通气),尽量避免试验过程中的溶剂蒸发所带来的试验数据上的变异。
FDA和EMA指南上建议使用的是人的离体皮肤,人体皮肤也被国外认为是IVPT 研究的金标准。国外人体皮肤通常来自于诸如整形手术(例如腹部整形术和乳房缩小术)、皮肤活检或尸体等途径。
国外人体皮肤通常是实验室与生物标本的商业供应商合作,这些供应商通常与多家医院和外科诊所签订协议,可以将人体皮肤(全层或皮肤切开)送到 IVPT 实验室以满足实验需求。在手术中心/医院采集后,会立即将皮肤转移到一个塑料容器中,该容器装有pH7.4的PBS溶液,在储存和运输过程中使用凝胶包,保持在4°C,运输过程中绝不能冷冻全层皮肤,因为这可能会影响解冻时的组织质量(皮肤完整性、活力或酶活性),IVPT 实验室收到全层皮肤后应立即进行处理。因此人体皮肤的供应量往往很低且价格昂贵。此外,每块皮肤都相对较小,通常每个供体最多只能满足6-8个扩散池使用。
因此当遇到使用人体皮肤应用受到限制、试验结果具有高度变异以及对皮肤渗透性低的药物和水溶液形式情况时,重组人体表皮(RhE)就适合成为人体皮肤的替代物,并已得到研究验证。RhE的优势还包括与人体皮肤相似,批次间的重现性更高,具有更高的通量率。
目前市售的RhE皮肤模型包括:EpiSkin®、SkinEthic®、EpiDerm®、LabSkin®和Phenion®FT。研究结果显示,这些RhE模型的渗透性均高于人体皮肤和猪皮,这主要是由于RhE皮肤屏障不完整所导致的。
RhE通常是由代表真皮的I型胶原蛋白基质制成,表面覆盖有IV型胶原蛋白膜,其上生长着源自人类角质形成细胞的分层分化表皮(即基底层、棘层、颗粒层和角质层)。这些细胞培养13天,面积通常为1.07 cm2。市售RhE产品都经过质量控制测试和组织学测试(即 HSE 染色的石蜡切片,以观察分化层并计算层数)、细胞活力(570 nm下的 MTT 测试)和屏障功能活性(使用Triton X-100 1%暴露时间诱导50%存活率)。
对于皮肤完整性的TEWL(经皮水分散失)测试,人体离体皮肤的TEWL值范围为10~20 g/cm2/h,通常将15 g/cm2/h作为皮肤完整性评价标准。但RhE的TEWL值通常高达30 g/cm2/h,具有较低的屏障阻隔功能。
另外需要注意的是,RhE通常是在培养基中,保持在37°C条件下来保证皮肤的的完整性和活力。但这与常规IVPT的32°C皮肤温度要求不符,但如果受试制剂和参比制剂在相同的的皮肤模型和相同的皮肤温度条件下测试IVPT,可以最大程度的降低温度差异所带来的偏差,这种做法目前已被监管机构所接受(例如,OECD)。
局部应用的半固体制剂不仅仅适用于皮肤治疗和妇科(阴道凝胶等应用于局部黏膜)领域,还包括眼科(眼用凝胶,软膏等)。
眼膏制剂具有一些独特的优势,例如增加角膜前停留时间、持续释放特性和缓解眼睛干涩等。因此眼科半固体制剂约占整体眼用剂型的11%,仅次于眼用溶液。
鉴于眼膏在眼表停留时间有限,且大多数眼科药物仅在眼表起局部作用,药物释放的速度和程度可影响药品的性能。另外一些病毒和细菌感染可能会在角膜内发展并进入虹膜、晶状体或眼睛的前房。因此,除了需要测定药物从制剂到眼表的释放外,还需要评估药物通过角膜的渗透速率和程度以及药物在角膜中的滞留量。
眼科半固体制剂IVPT研究采用的膜材是兔子的角膜。通常是取新西兰雄性白兔的新鲜角膜(24小时内),每个角膜都单独储存在隐形眼镜盒内,并在运输期间和接收时都保持在4°C。所有角膜都要在取出后3天内使用,以减少储存期间角膜上皮的潜在损伤。在实验开始前和实验结束时,在接收后立即检查角膜的形态,包括其透明度。实验仅使用透明角膜,实验结束时角膜应未见任何变化。
IVPT装置上与常规垂直扩散池不同,应使用带球形接头的垂直 Franz 扩散池(详见下图),以迎合角膜的曲率弧度的要求。此外试验中建议使用Parafilm覆盖上药后的供给池,以减少试验过程中的统计蒸发。扩散池恒温控制在 37.0±0.5°C。
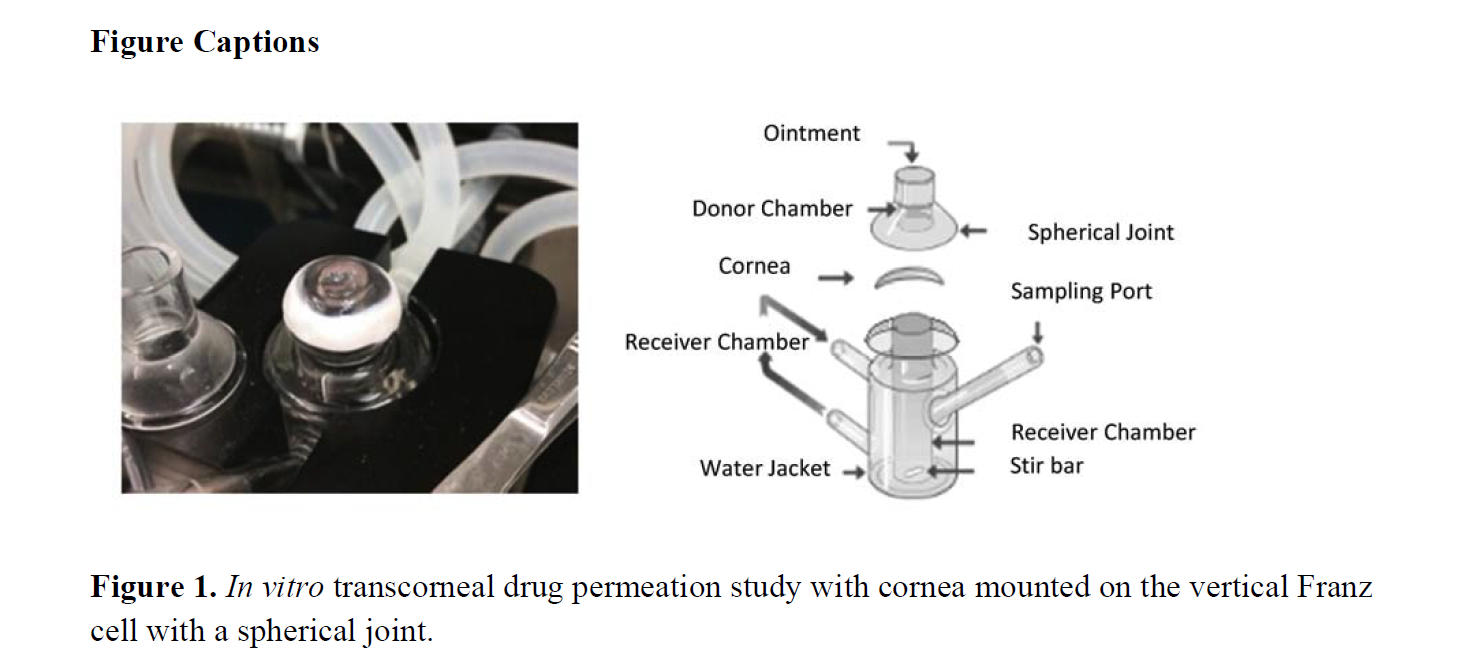
Al-Ghabeish, Manar, Xu, Xiaoming, Krishnaiah,Yellela S.R., Rahman, Ziyaur, Yang, Yang, Khan, Mansoor A., Influenceof drug loading and type of ointment base on the in vitro performanceof acyclovir ophthalmic ointment.International Journal of Pharmaceutics.http://dx.doi.org/10.1016/j.ijpharm.2015.08.096
下期讲讲IVPT和BE的关联性,两个试验哪个更严格?敬请期待。
一、服务范围:
-
皮肤外用制剂配方的开发与优化
-
BE和生物利用度评价
-
仿制药Q3一致性对比研究
二、团队介绍
核心团队拥有各种类型外用制剂的体外释放和体外透皮的研发经验,同时拥有完整的质量控制体系和完善的实验设计操作管理体系。
三、设备概况
实验室配备了适用于生物分析及体外透皮的一整套先进分析设备,其中包括LC-MSMS、GC-MS、ICP-MS、HPLC、IC、LOGAN全自动体外透皮扩散系统、高通量组织研磨机等仪器设备,可提供多种检测及研发服务。
四、实验流程标准化
对于控制实验结果变异,安徽安邦医药IVPT服务平台目前已建立标准化的控制标准,严格控制实验变异源。拥有独立的统计部门进行数据处理与分析,提供科学有效的统计数据。
五、项目经验
已完成上百个生物样本分析项目,并完成多个项目的IVPT研究,助力合作伙伴成功申报。
附图:

LOGAN体外透皮扩散系统

LC-MSMS(Thermo Fisher)
LC-MSMS(AB SCIEX 5500)

经表皮水分丢失量测量仪
欢迎来自全国各地的伙伴合作咨询。
交流洽谈:范经理
联系方式:13635699896(微信同号)
交流洽谈:王经理
联系方式:15156091013(微信同号)
|
